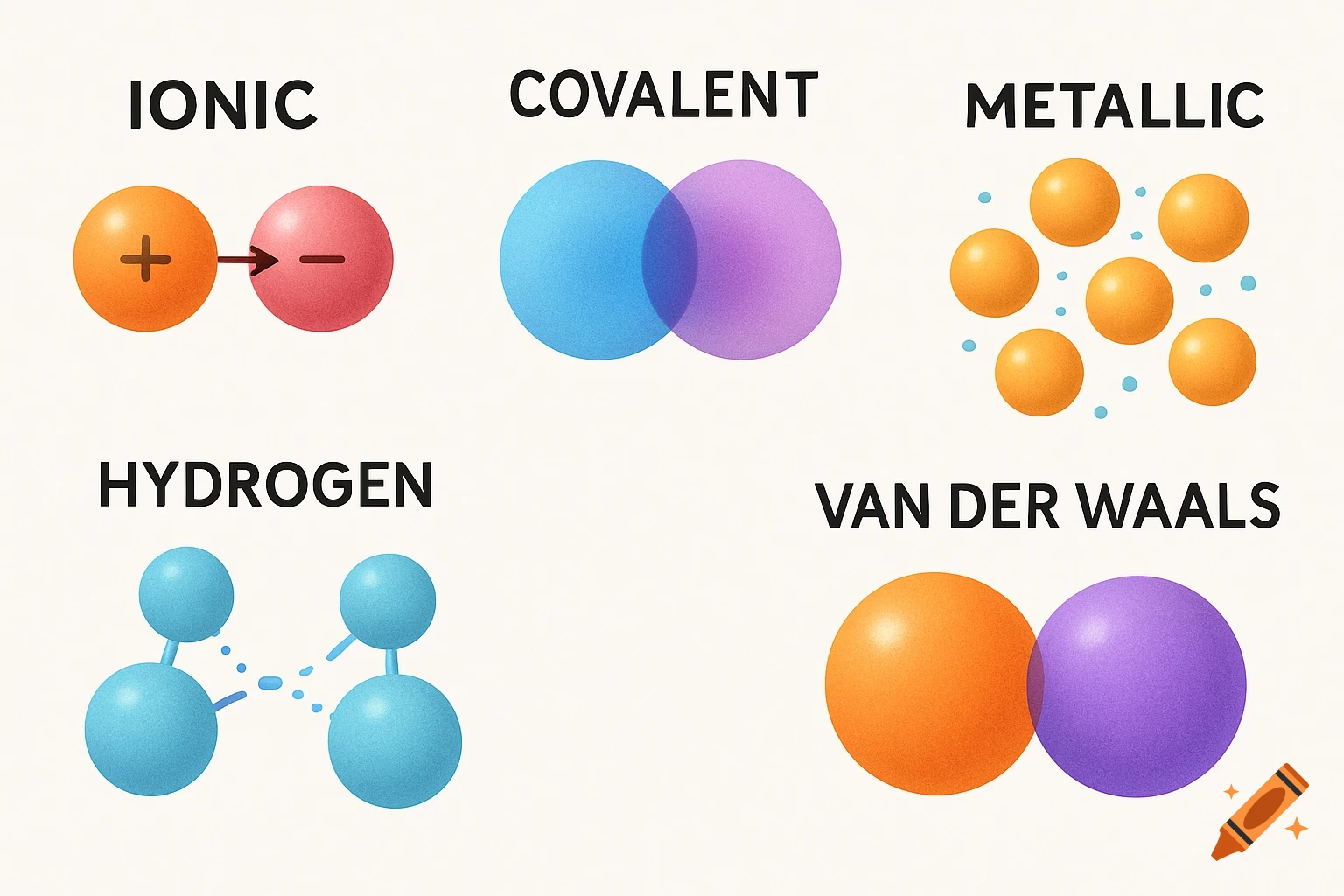
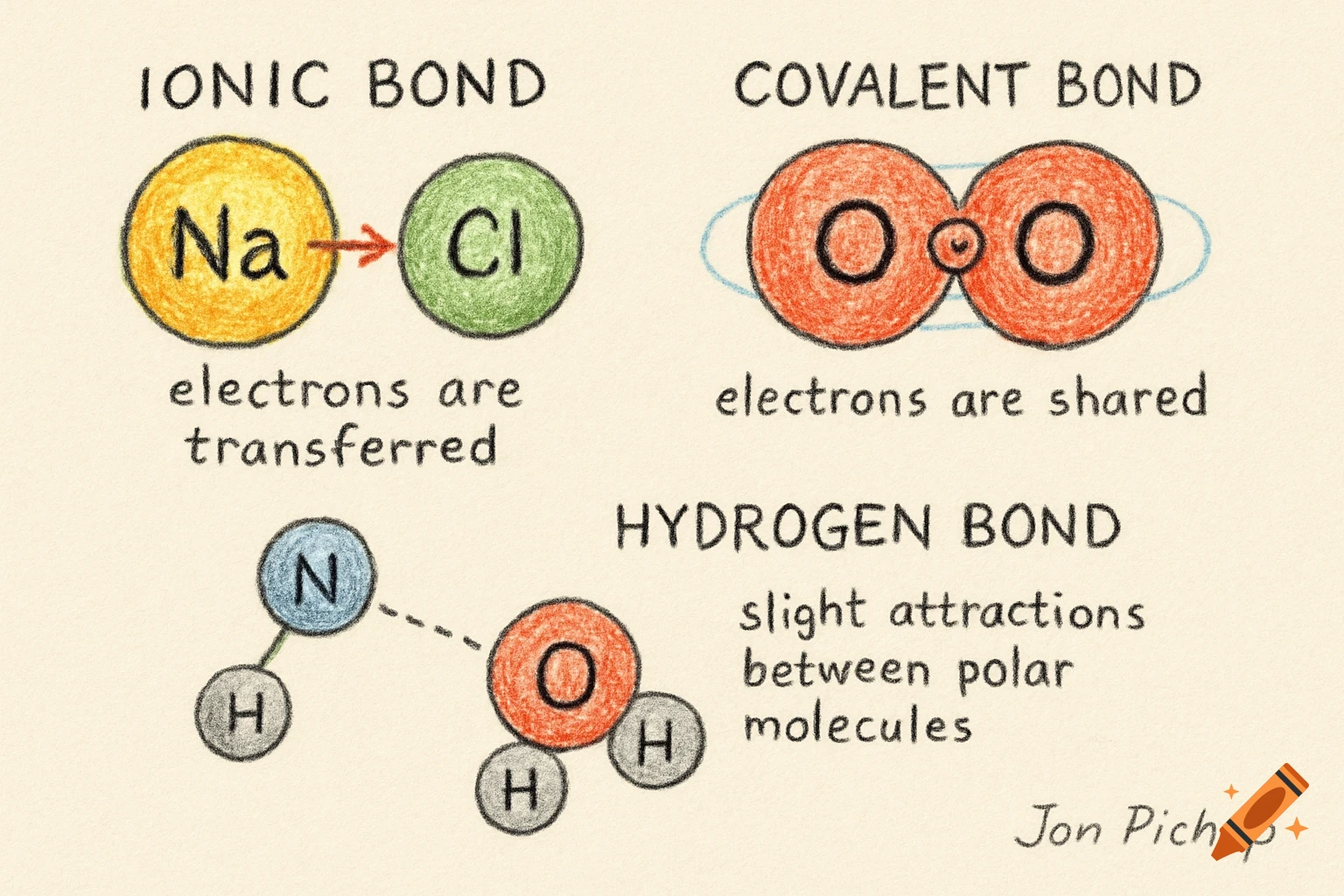
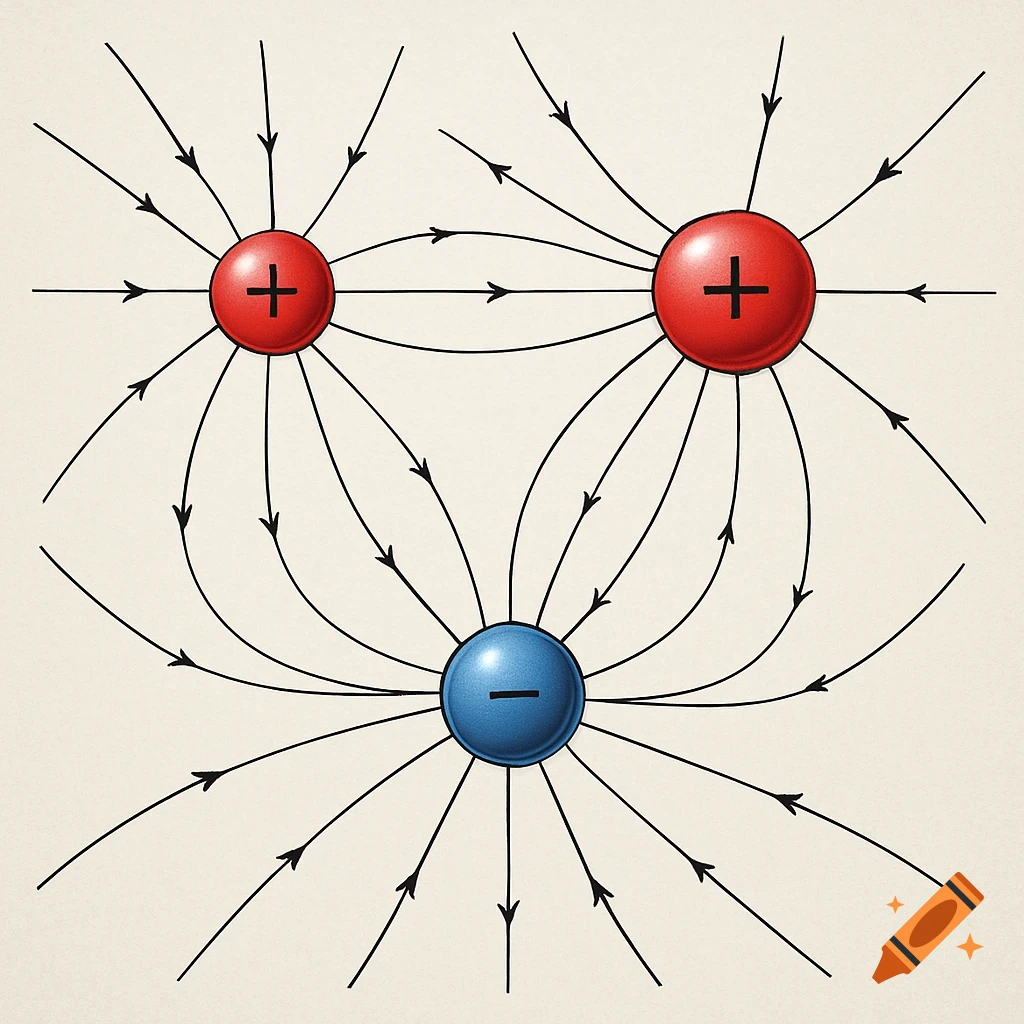
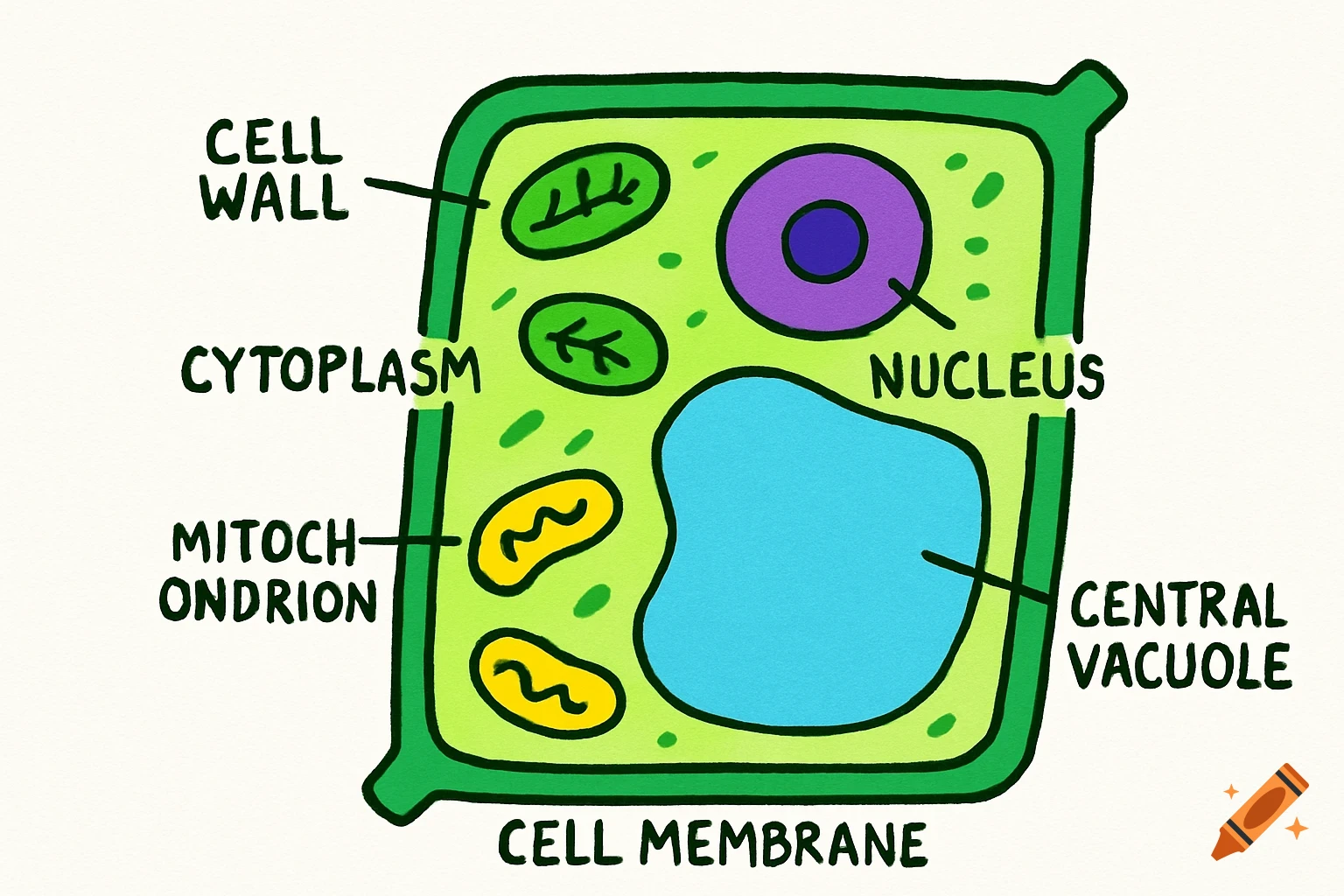
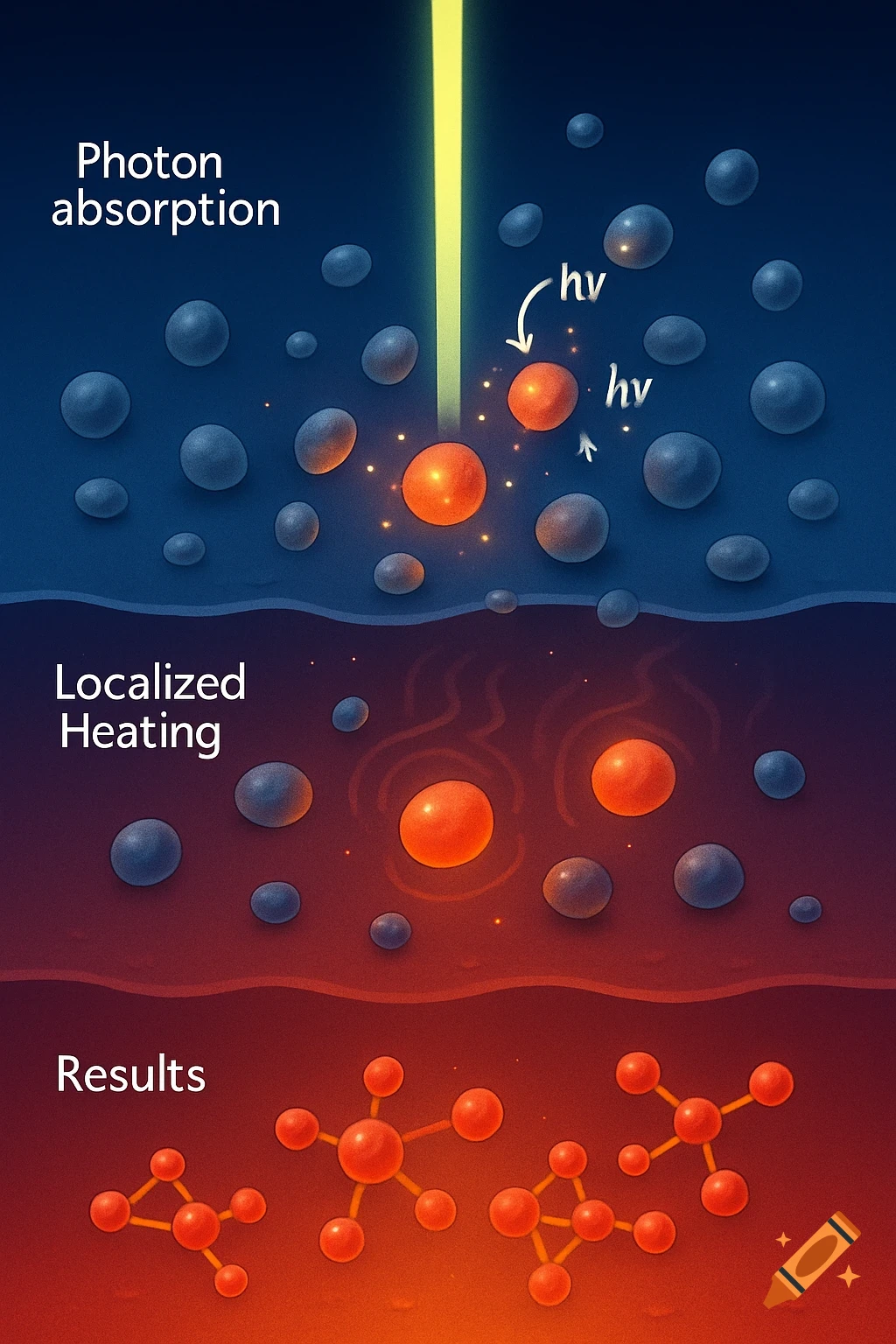
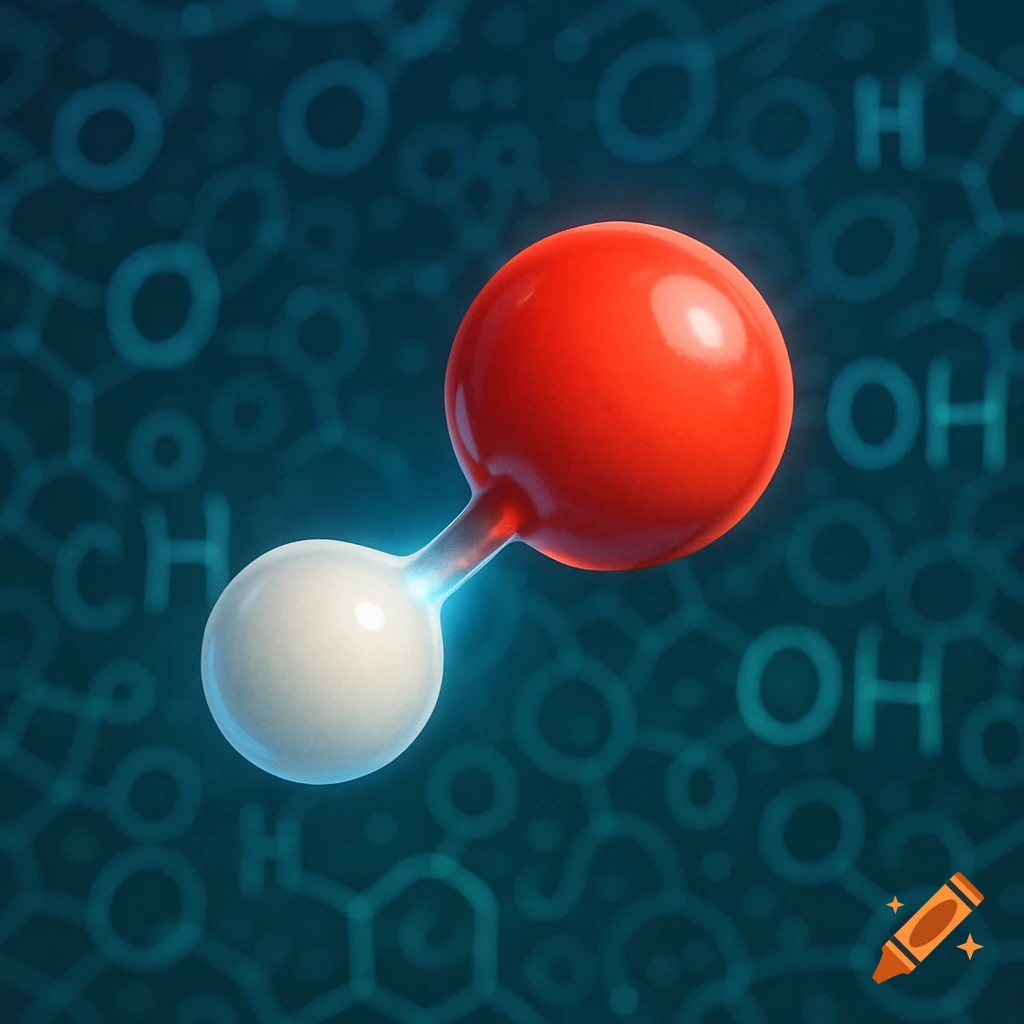
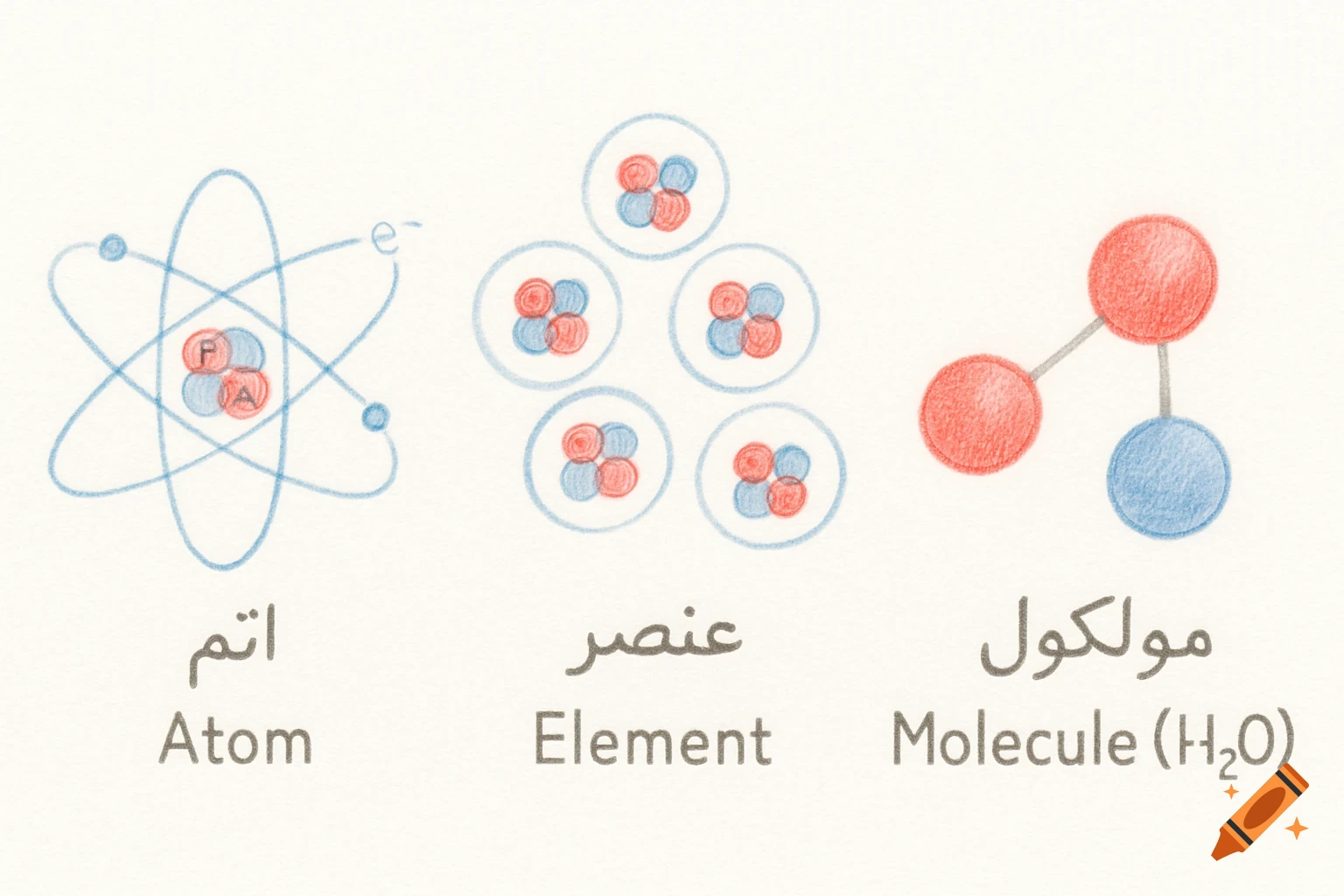
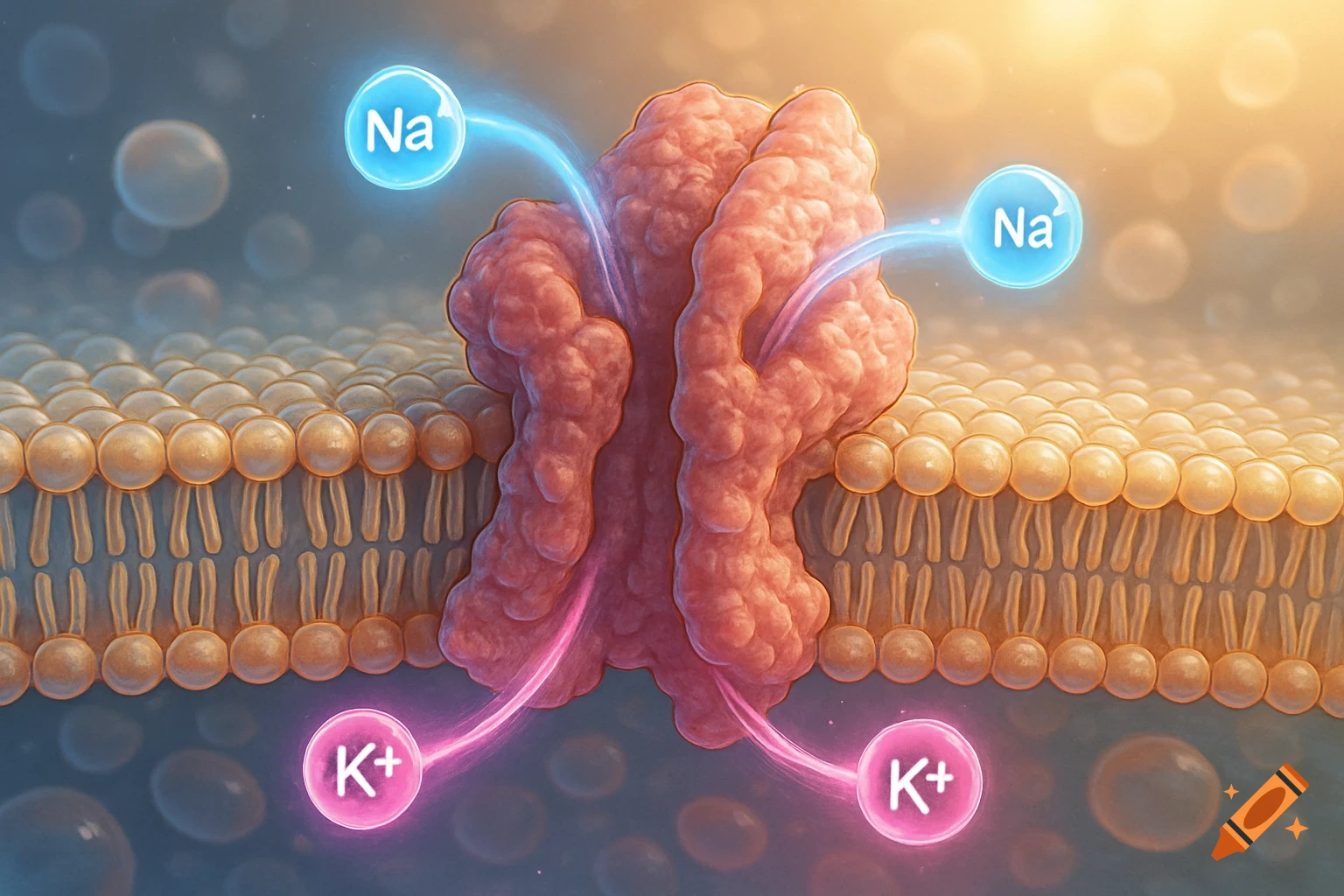
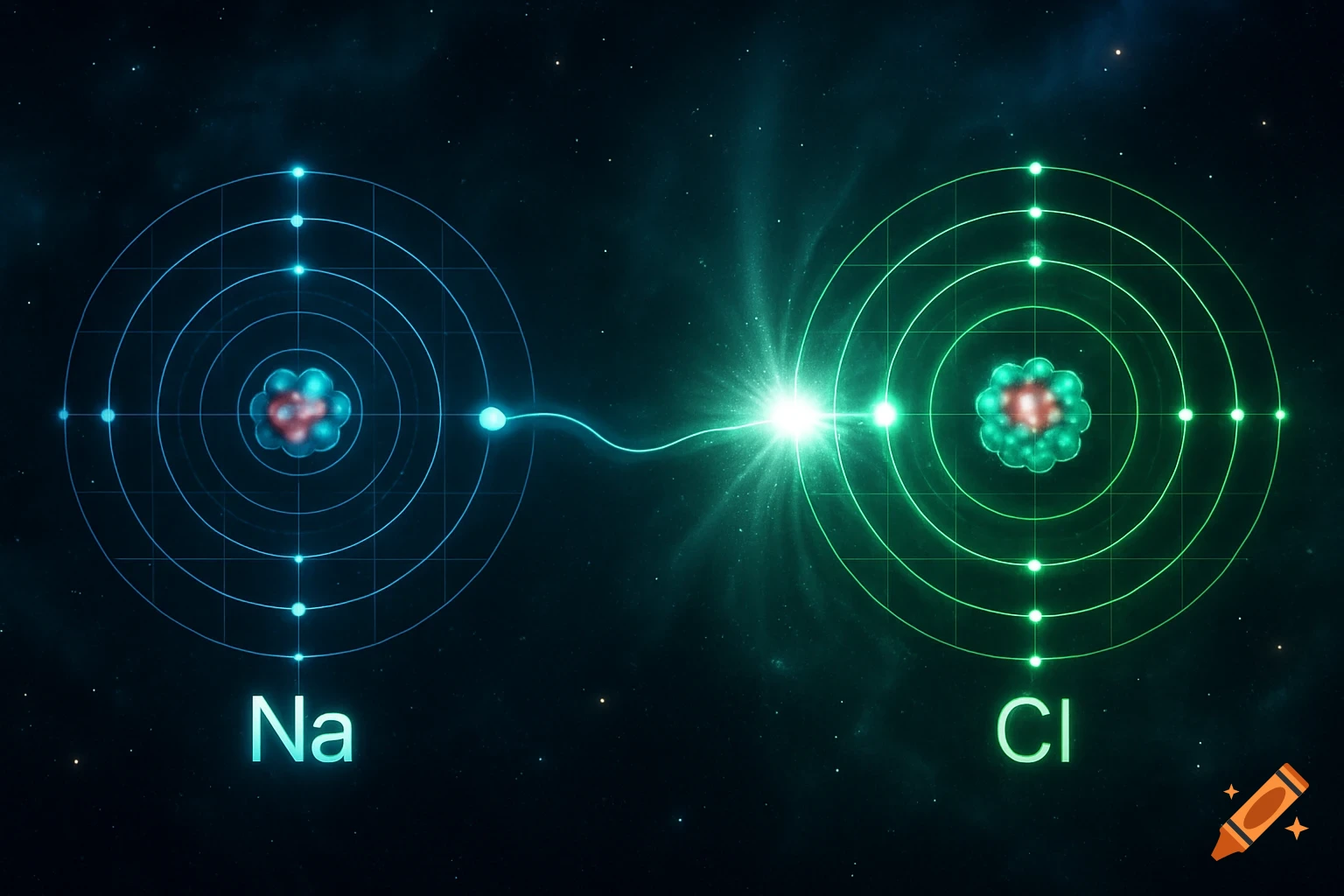
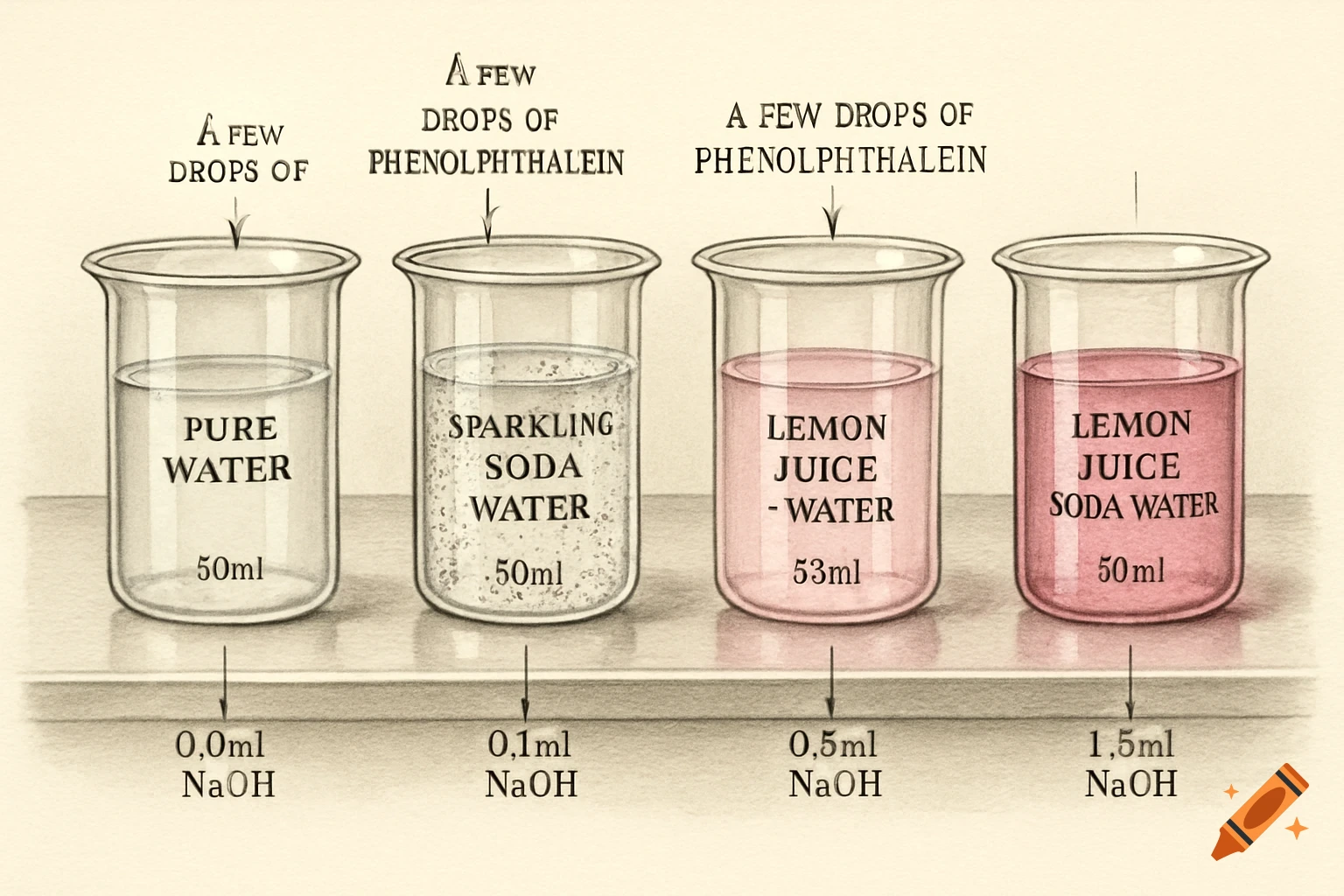
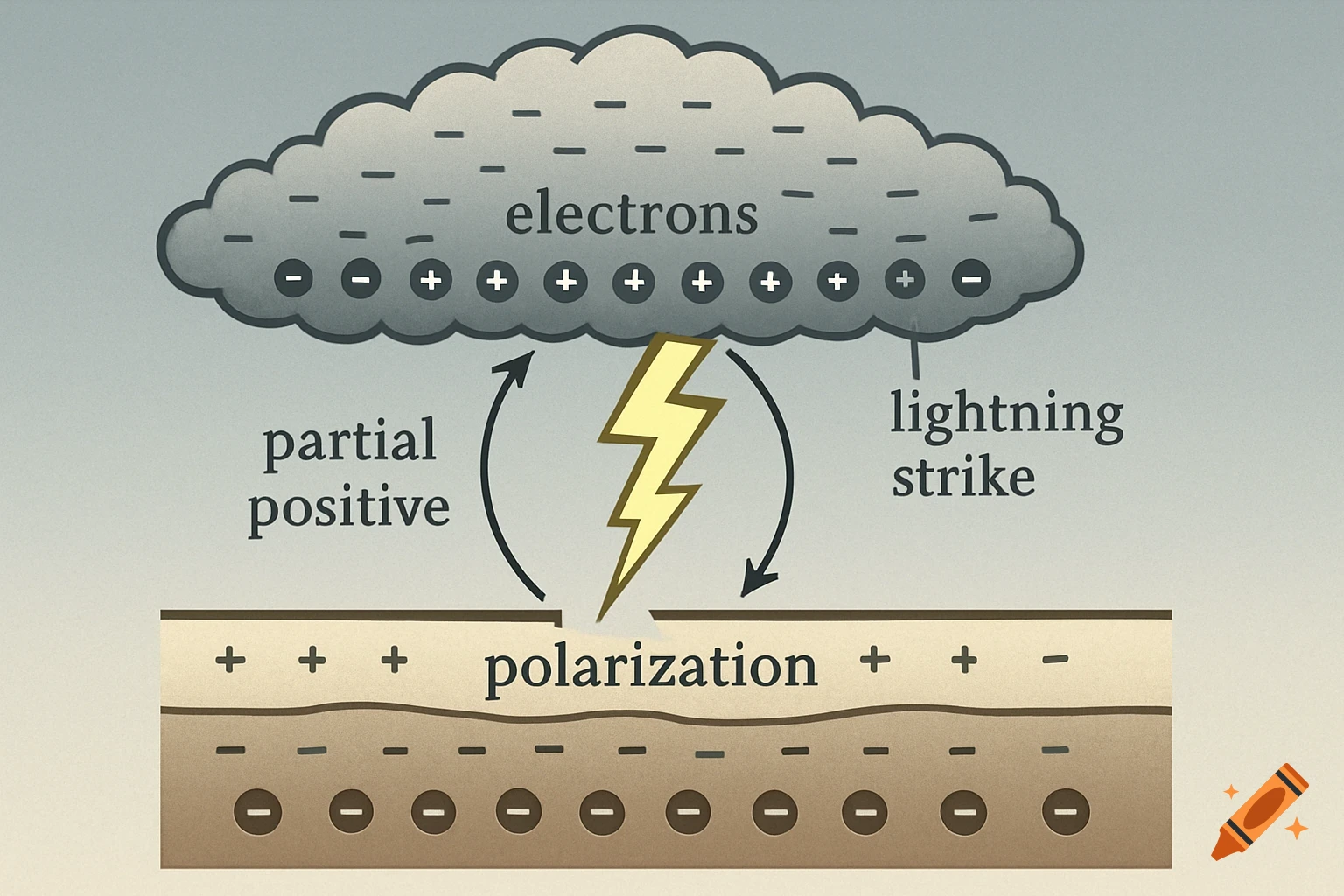
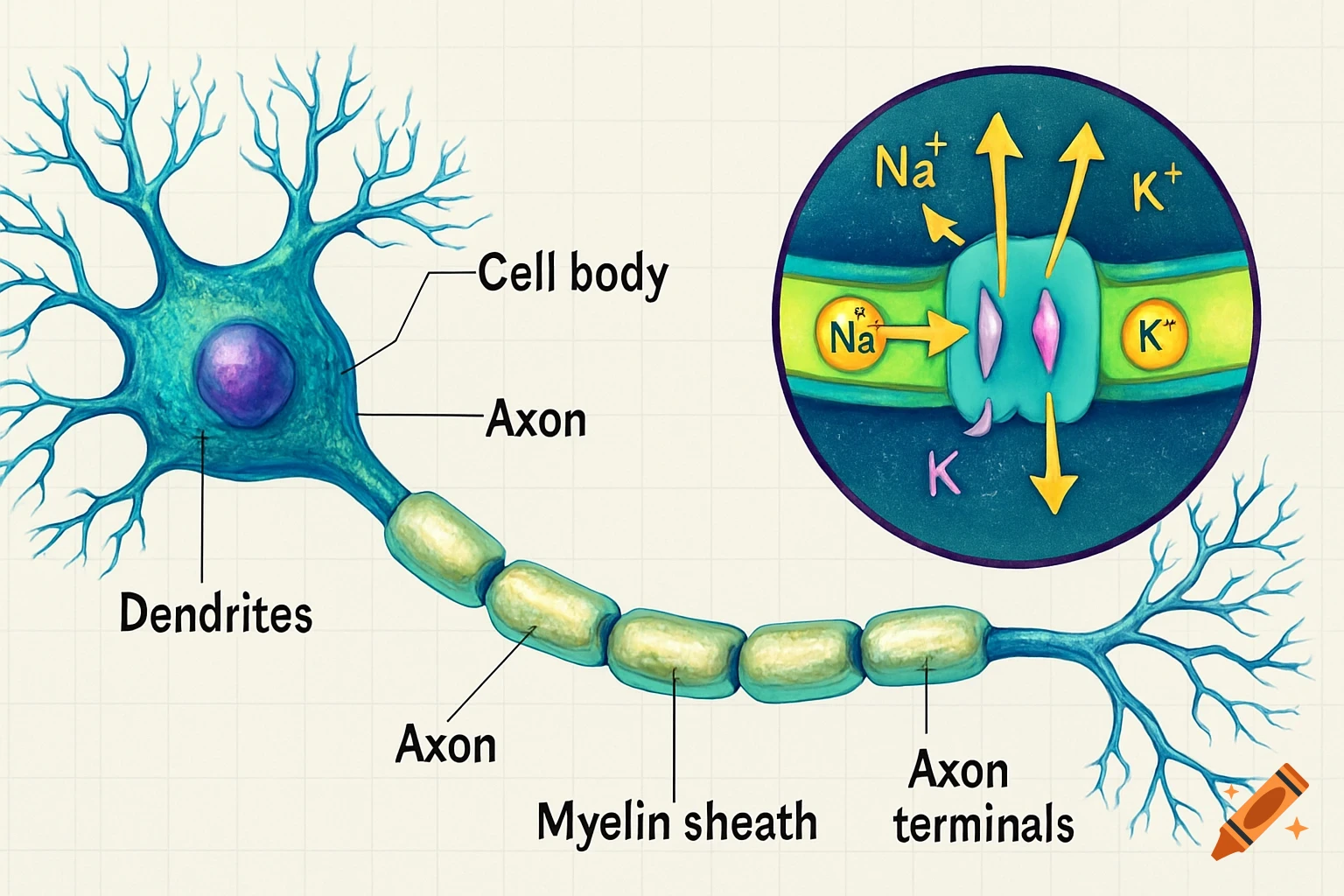
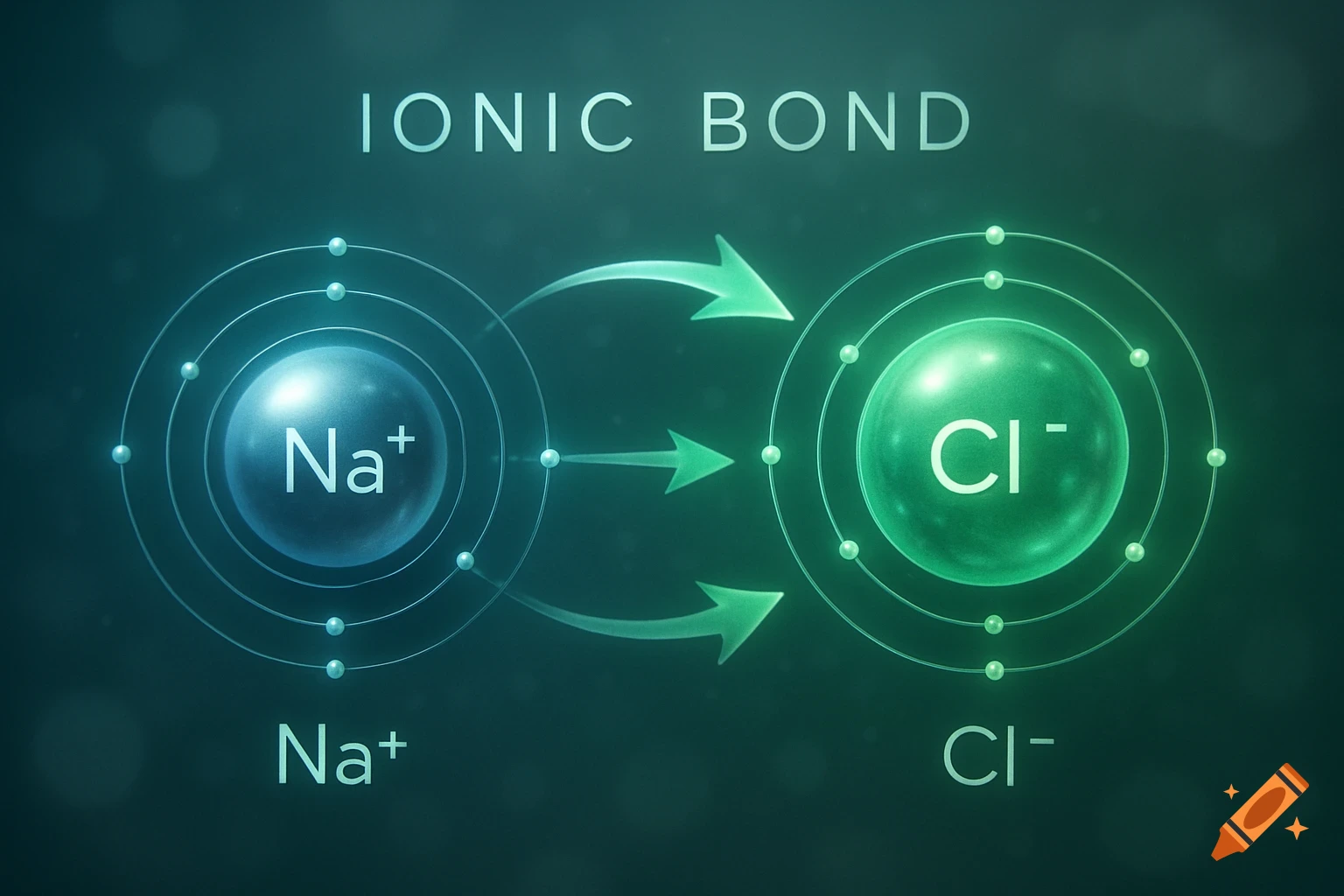
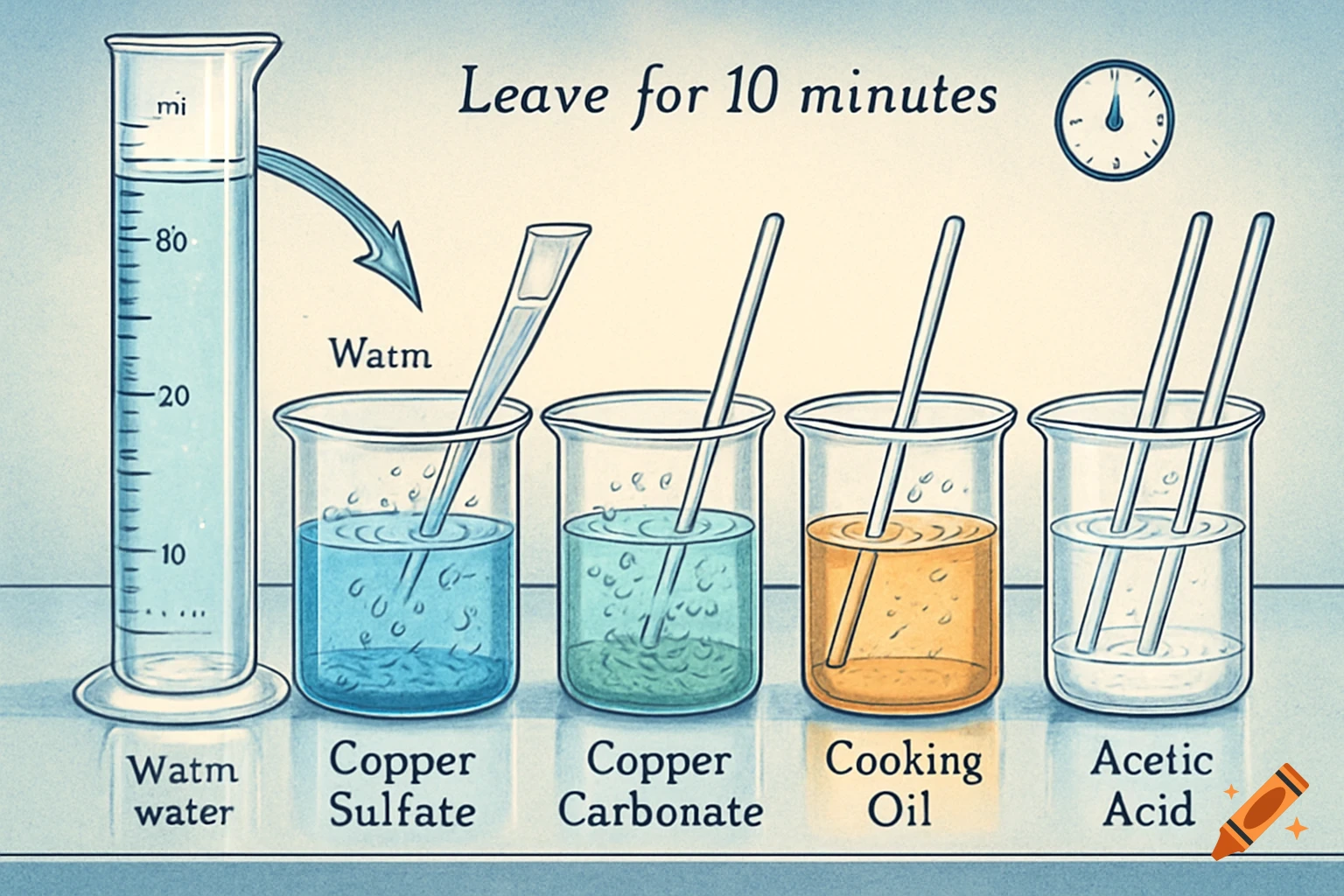
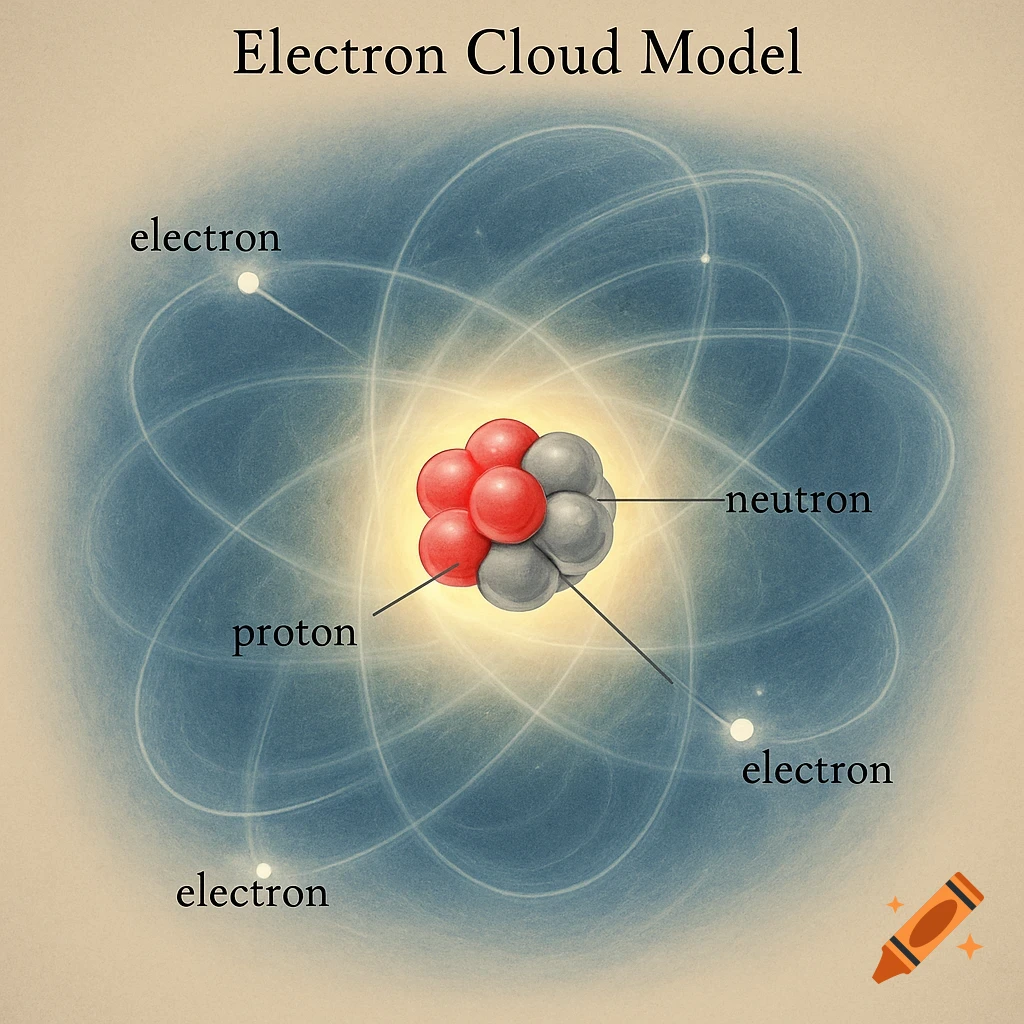
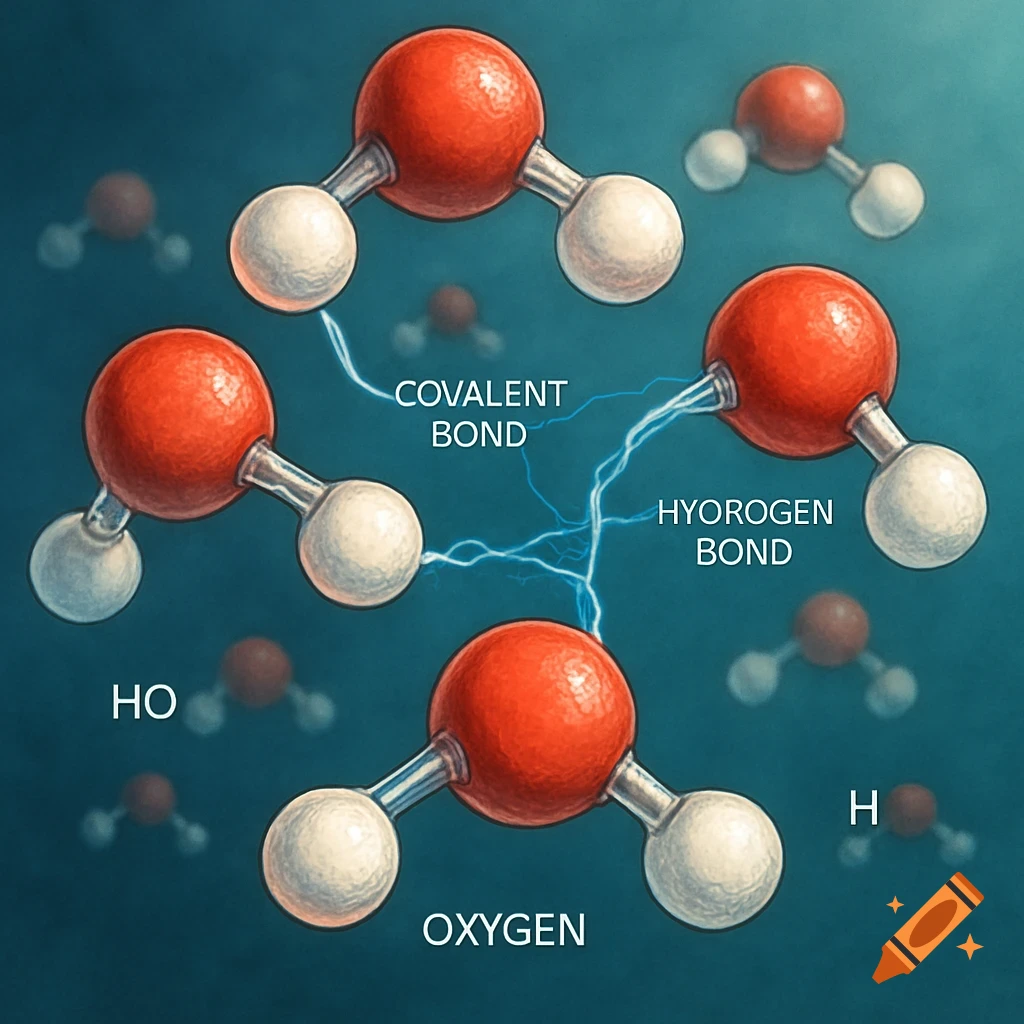
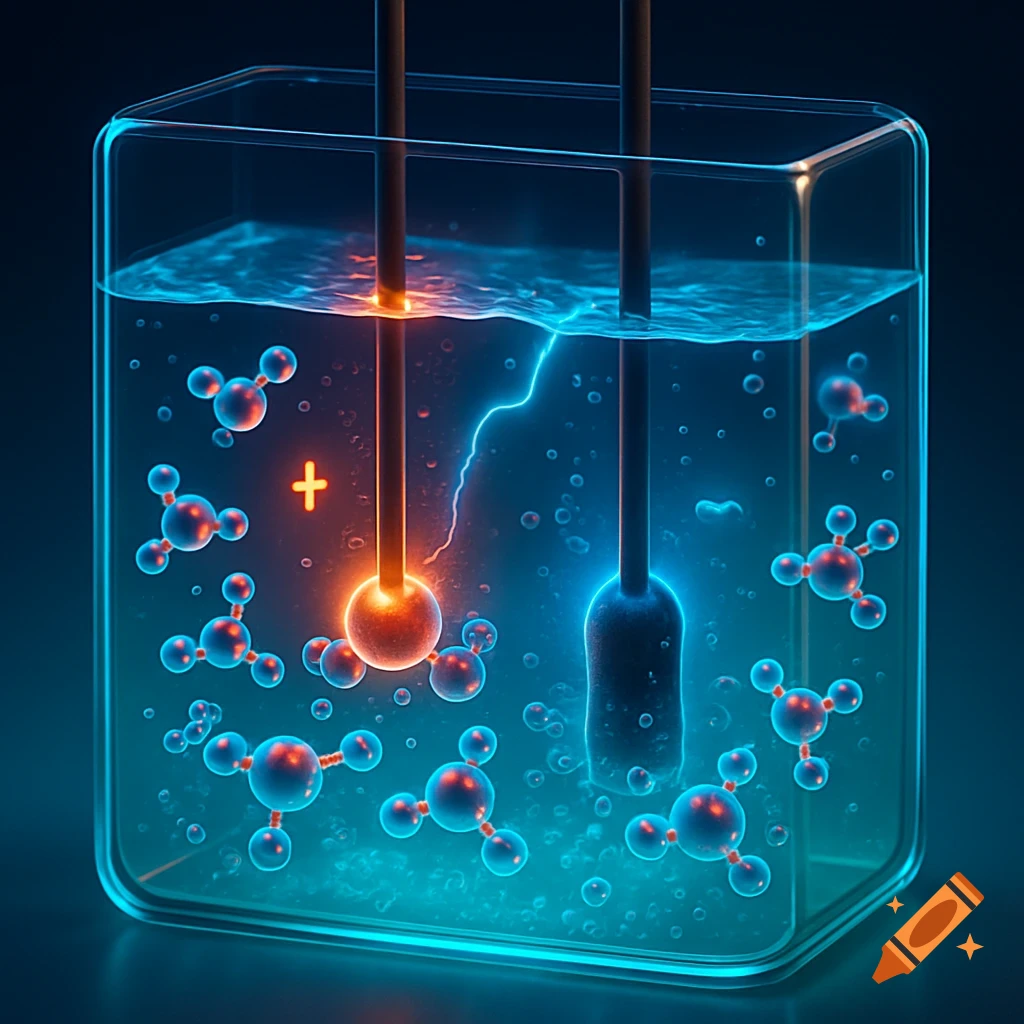
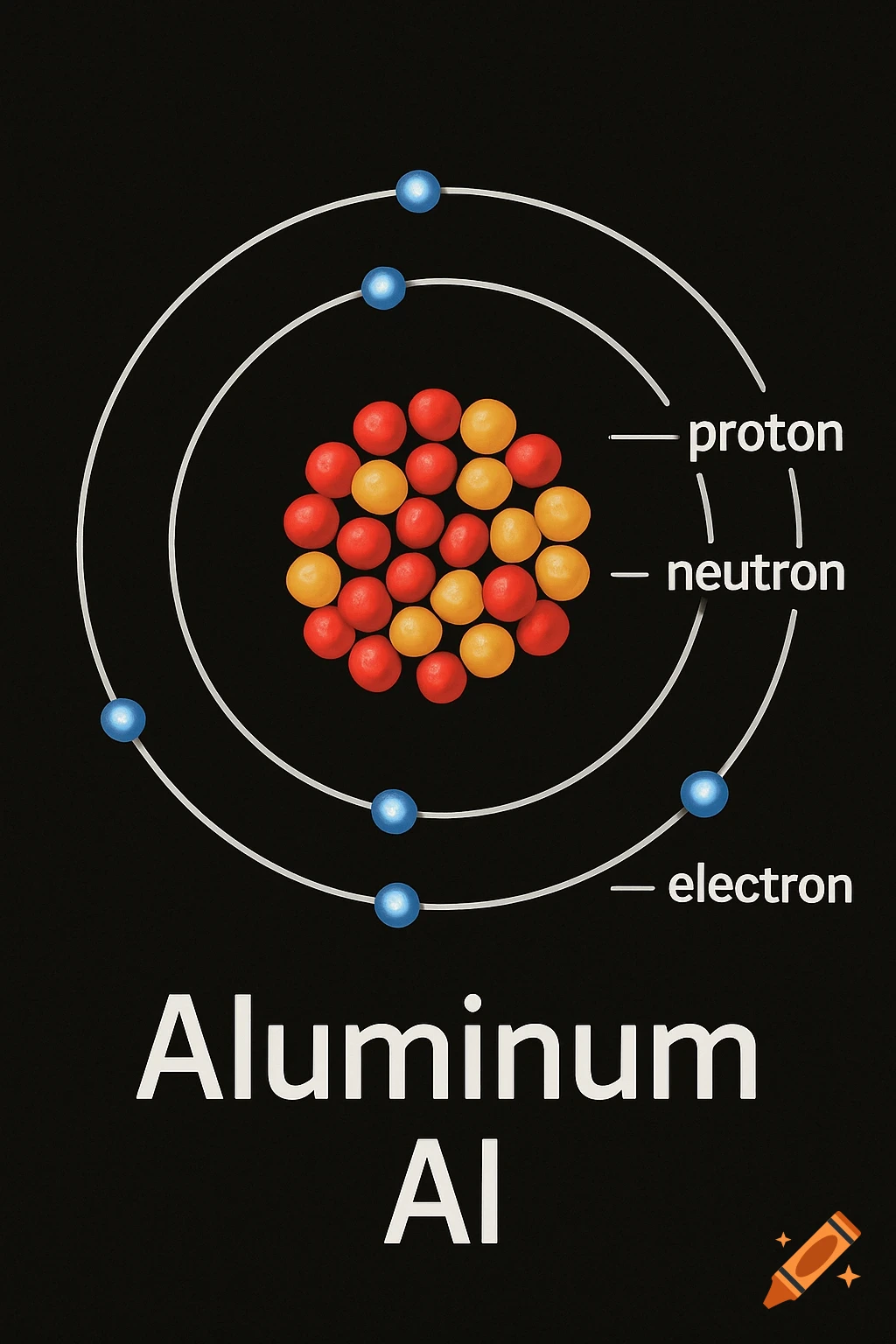
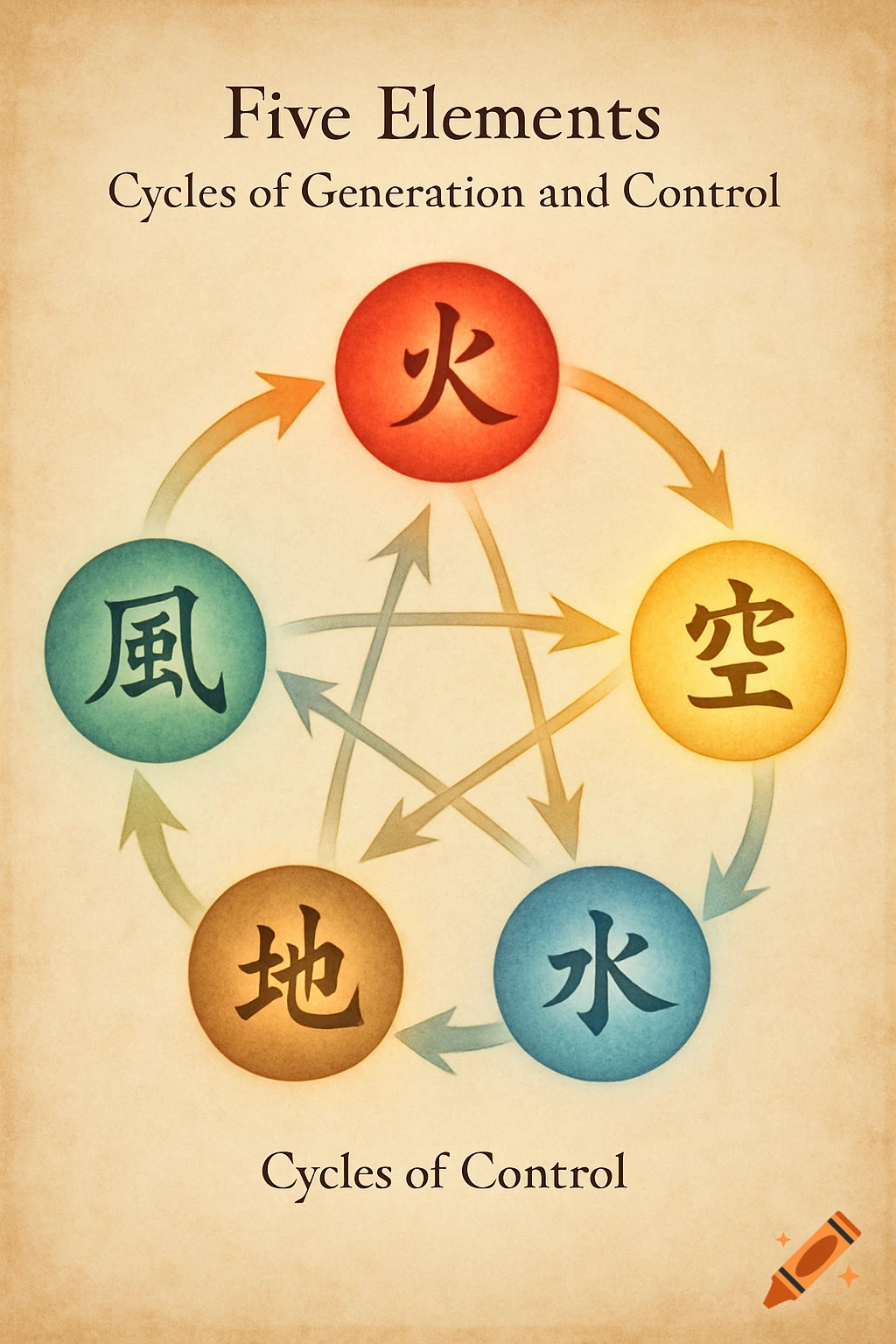
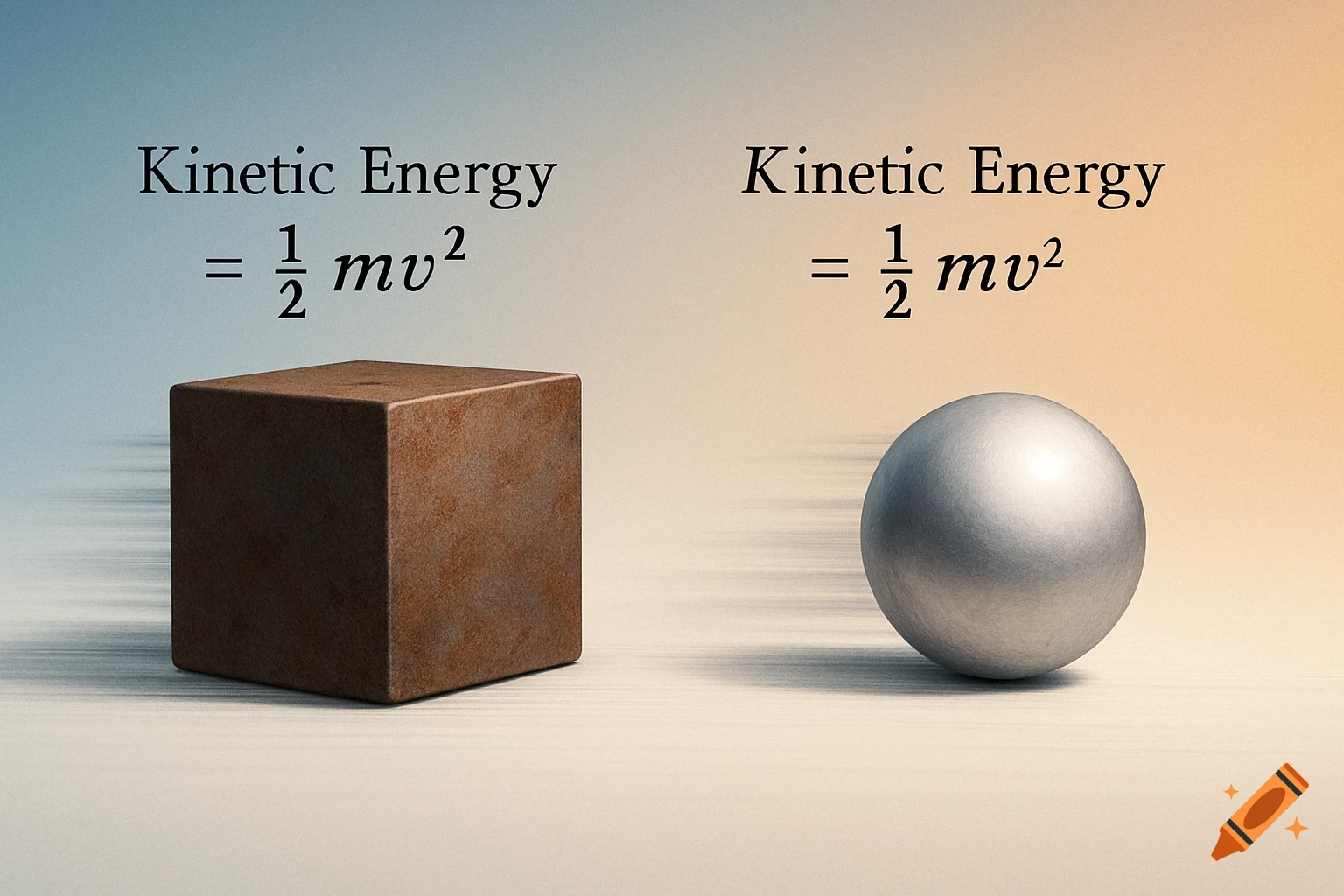Diagrams illustrating properties of water: polarity, hydrogen bonding, solubility, and special properties like density differences between liquid water and ice, with chemical structures and labels.
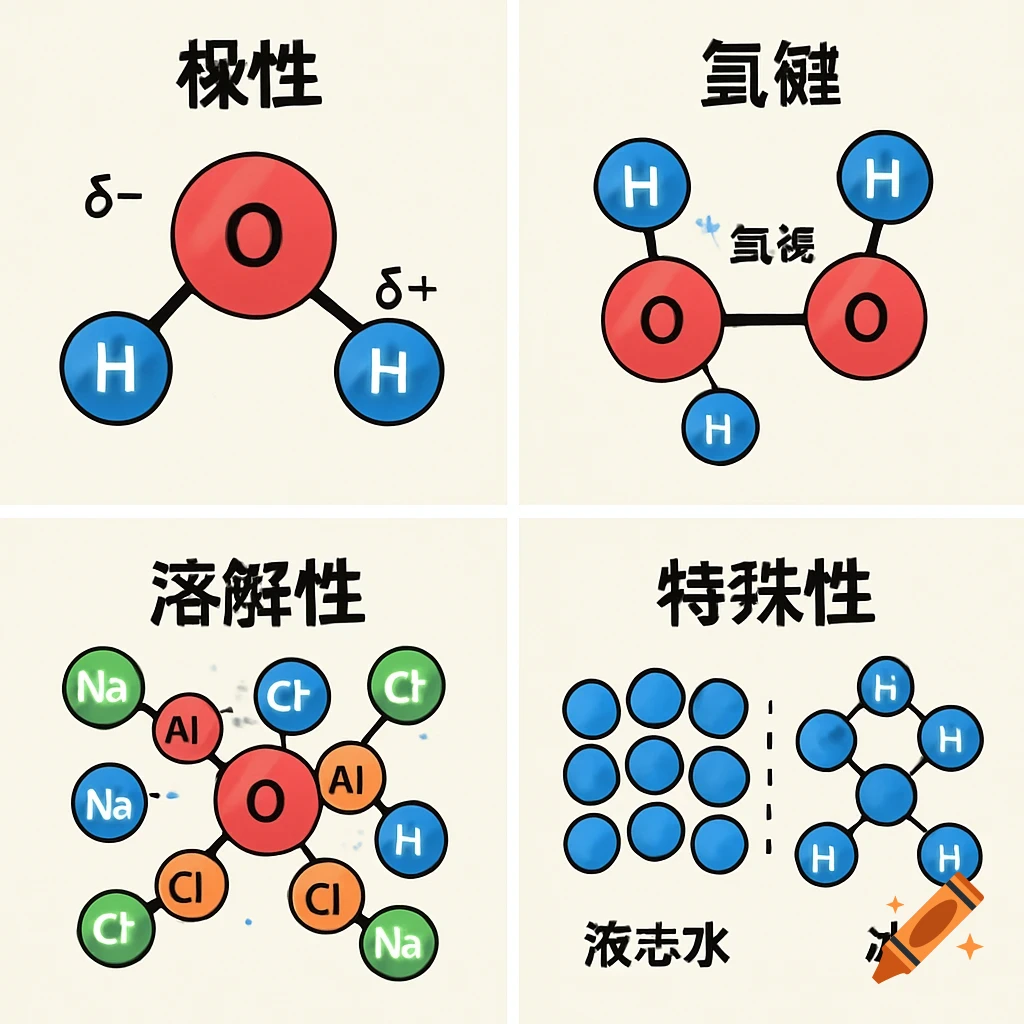
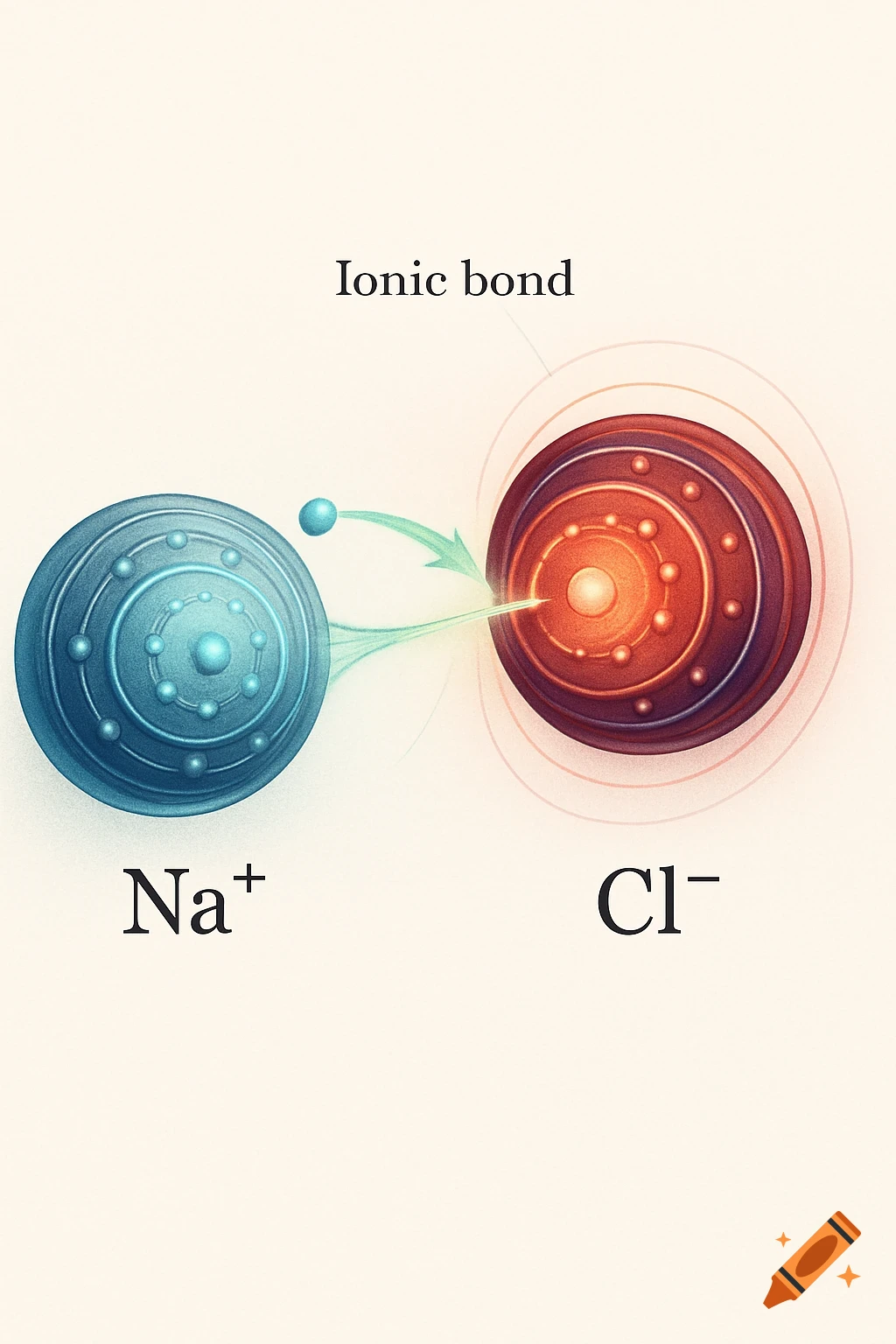
1. 水分子是极性分子,就是说水分子的一遍有负电荷(氧原子)另外一边是正电荷,氢原子, 可以让水和其他极性分子或者带电分子发生相应的反应,比如说水溶解盐,因为盐的正负离子可以和水的极性分子结合。就是说水分子有极性,有正负两端。2. 氢键=水分子之间的吸引力,很弱,但是很重要,就是水分子原子的正电荷和负电荷之间互相吸引,所以说氢键可以让水有高表张力,较高的比热容量,能够吸热蒸发等等。意思就是说,氢键 是因为水分子的极性(正电荷,负电荷)然后有吸引, 就会让水有高表张力等。3. 水的溶解性,水被称为所谓的“万能溶剂” 能溶解很多物质,特别是极性分子和带电粒子,能够和带电物质发生相互的作用。比如说水能溶解盐, 因为盐的离子与水分子之间形成氢键。就是说水能溶解很多物质,包括极性分子和离子。4. 水的特殊性: 比如说高比热,就是说水的整体温度变化小。蒸发热高,水在蒸发的时候需要大量热量, 帮助地球调节温度。水的密度高冰,因为冰在水中,水中的生物有较为温暖的环境,为什么密度比水低的原因也是因为冰的分子更散。 See more